2019年 | プレスリリース・研究成果
東北メディカル・メガバンク計画参加者における先天性代謝異常症の原因バリアントの保因者の頻度を推定 ~日本人一般集団における遺伝性疾患の理解へ向けて~
【発表のポイント】
- 日本人の全ゲノムリファレンスパネル*1を用いて、先天性代謝異常症*2について原因遺伝子の病的バリアントの保因者*3の頻度を初めて推定し、ゲノムの多様性から劣性遺伝性疾患*4の有病率の推定に取り組みました。
- 日本で新生児スクリーニング*5対象となっている17の先天性代謝異常症の32の原因遺伝子について推定を行い、その結果、フェニルケトン尿症*6やCPT2欠損症*7において現実の有病率からの推定値と近い値を示し、ゲノムの多様性からの推定が可能であることを示唆しました。
- しかしながら、ゲノムおよび有病率からの保因者頻度の推定の比較結果は疾患ごとに異なり、病的バリアントの発症への効果の程度が未解明であることや、検出されていない病的バリアントが存在する、などの要因が示唆されました。
- 今後データの拡充やバリアント解釈*8法の進展などにより解明がさらに進むと、ゲノムのデータから一般集団での遺伝性疾患の潜在的な患者の割合の推定に役立つと期待されます。
【概要】
遺伝性疾患は、形質のあらわれ方や家系での発症者のあらわれ方によって、何種類かに分類することができます。ヒトは、一人ひとりが両親からの2セットの遺伝情報を持っているので、疾患の原因遺伝子についても2つのコピーを持っています。優性(顕性)の遺伝性疾患は、疾患を起こす変異型を1コピーでも持っていれば、発症します。一方で劣性(潜性)の遺伝性疾患は、2コピー双方に機能欠損を起こす変異があり、その遺伝子の本来の機能を発揮するコピーが無いときに、疾患などの形質があらわれます。劣性の遺伝性疾患は、原因となる遺伝子の変異を2コピー双方に持つことで発症しますが、それを片方だけ持つ状態を「保因者」と呼びます。しかし、保因者の集団中での頻度が疾患ごとにどの程度であるのかは、はっきりとはわかっていませんでした。疾患ごとに、発症者の頻度(有病率)が分かっている場合は、保因者の頻度は計算により推定可能ですが、実際に劣性の遺伝性疾患の原因変異を持つ人が一般集団中にどれくらいの割合で存在するかについては、これまで解明が困難でありました。
東北大学東北メディカル・メガバンク機構(ToMMo)では、日本人の全ゲノム解読を大規模に行い、全ゲノムリファレンスパネル(現在3,552人で、3.5KJPNv2と呼ぶ)を構築して、ゲノムのバリアントの頻度情報を国内外に公開しています。このパネルには、対象となった日本人において各バリアントがどれだけの頻度で存在するかのデータが含まれています。本研究では、3.5KJPNv2のデータを用いて、集団のゲノムの多様性は遺伝性疾患の有病率をどれくらい推定できるのか、という課題に取り組みました。具体的には劣性の遺伝性疾患である、先天性代謝異常症疾患の原因バリアントの検出と保因者の頻度の推定を行い、各疾患の検査での陽性の人の割合に基づく既報の有病率との比較を行いました。
今回の研究で着目した遺伝性疾患は、フェニルケトン尿症など、原因遺伝子が分かっている17の先天性代謝異常症で、劣性(潜性)遺伝病です。これらの疾患は、治療法があり生化学的検査の精度が高いことなどから、新生児のスクリーニング対象として優先順位が高くなっています。そのため、多数の新生児が検査を受けており、疾患が見つかった割合について精度の高い統計データがあります。
本研究では、この17の疾患の原因として知られている32の遺伝子を解析対象としました。3.5KJPNv2のバリアント全体について生物・医学的アノテーション*9とバリアント解釈を行い、32の遺伝子について、既報および推定された病的バリアント検出を4種類の方法で行いました。検出された病的バリアントとそれらの頻度を用いて、保因者の頻度の推定を行いました。一方で、過去の新生児スクリーニングで報告されている有病率から理論的に推定される保因者の頻度を得て、比較を行いました。4種類の病的バリアントの検出法に基づくゲノム変異の保因者の頻度を推定し、フェニルケトン尿症やCPT2欠損症などの酵素欠損症では、有病率から推定された値と近い値を示しました。このことは、ゲノムデータより有病率を推定することが可能であることを示唆します。
しかしながら、ゲノムデータと有病率から推定された保因者頻度の比較結果は、疾患ごとに異なっていました。違いや推定値のずれを生んだ要因としては、ゲノムからの推定値の方が高ければ、バリアントの発症への効果の程度が未解明であるなどの理由、一方でゲノムからの推定値の方が低ければ、病的バリアントは他にも存在する、などの理由が考えられます。今後、更に研究を進めるにあたって、特に、1)研究の進展に伴い知見が増えると病的バリアントと判断されるものは増加する、2)個々の病的バリアントが特定の遺伝子型で実際に発病に至る割合については未解明であること、3)頻度が高めのバリアントであっても他の病的バリアントとの共存状態で発病に貢献することがあり集団中の患者の割合に影響し得る、などに注意を払う必要があります。
本研究は、ヒト集団のゲノムの多様性が劣性の遺伝性疾患の有病率をどれくらい説明できるのかについての初めての取組でしたが、今後、ゲノムデータと有病率それぞれに基づく保因者の頻度推定結果で違いが生じる方向と程度を明らかにしていくことで、ゲノムのバリアント頻度と一般集団中の潜在的な患者数の割合との関係の理解が進むと期待できます。
東北メディカル・メガバンク計画は、平成27年度より、国立研究開発法人 日本医療研究開発機構(AMED)が本計画の研究支援担当機関の役割を果たしています。本計画の事業の実施は、東北大学東北メディカル・メガバンク機構(ToMMo)と岩手医科大学いわて東北メディカル・メガバンク機構(IMM)とが連携して行っています。
【用語解説】
*1 全ゲノムリファレンスパネル3.5KJPNv2:東北メディカル・メガバンク計画で実施された、一般の日本人3,552人の全ゲノム解読により、検出されたゲノムのバリアントから構築された日本人ゲノムの変異パネル。バリアントの頻度情報は、jMorp (https://jmorp.megabank.tohoku.ac.jp/) より公開されている。https://www.megabank.tohoku.ac.jp/news/27839
*2 先天性代謝異常症: 生まれつきの遺伝的な要因により、体の構成成分の新陳代謝やエネルギー産生の代謝の一部が機能しなくなっていることによって、発症する疾患。遺伝性の代謝機能の欠損の多くは、代謝に関わる特定の酵素や分子をコードする遺伝子に変異があることで機能欠損型となっている。
*3 保因者(キャリア): ここでは常染色体劣性(潜性)の遺伝性疾患において、病気の原因となる遺伝要因を一つ、片方の染色体でのみ、ヘテロの状態で保有している人のこと。もう片方の染色上の該当遺伝子の産物が正常な機能を発揮していれば、発症しない。
*4 劣性(潜性)遺伝性疾患: メンデル遺伝性疾患の特定の原因遺伝子において、父方由来と母方由来の両方(2コピー)が、ともに機能欠損のタイプであり、正常の機能を発揮するコピーを持たないときに、発症する遺伝性疾患。家系では、世代をスキップして発病者が現れる。直近の遺伝学用語改訂(日本遺伝学会)では、検討を経て、劣性を潜性へ(そして優性を顕性へ)と改訂している。
*5 新生児スクリーニング: 先天性代謝疾患や先天性内分泌疾患の早期発見および早期治療を可能にするため、新生児を対象に、生まれて数日後の血液を用いて行われる検査。歴史的には、フェニルケトン尿症の検出から始まり、生物学的な手法により検査が行われてきた。最近では、質量分析法を活用したタンデム・マス試験が導入されており、多種類の代謝物を短時間に測定できるようになった。日本でのタンデム・マス試験一次対象疾患の16疾患は、治療法が確立しており、かつ検査の精度が高い、などの理由で選ばれている。二次対象疾患は、検査対象としての追加が検討されているものであり、CPT2欠損症などが含まれる。
*6 フェニルケトン尿症:アミノ酸代謝異常症の一つ。フェニルアラニンをチロシンに変換する酵素(フェニルアラニン水酸化酵素)の機能欠損のため、身体にフェニルアラニンが蓄積し、チロシンが少なくなる。血中のフェニルアラニンの濃度が高い状態が続くと、発達遅滞などの神経症状を示す。チロシンの欠乏により、色素産生に影響するので、髪や皮膚の色が薄くなる。過剰なフェニルアラニンは、フェニルケトン体として尿中に排泄されるため、フェニルケトン尿症として知られている。
*7 CPT2欠損症:カルニチンパルミトイルトランスフェラーゼ-2 欠損症。体内で脂肪を分解できないために、エネルギーとして活用することができない、脂肪酸代謝異常症の一つ。エネルギー産生不全に陥ることが、重篤な低血糖症状につながる。そしてエネルギーを必要とする脳や筋肉に影響するため、意識障害、痙攣、などの症状を示し、時には突然死に至ることもある。新生児スクリーニングでは二次対象疾患と位置づけられてきたが、最近では重要視されていている。
*8 バリアント解釈: 遺伝子のバリアントが病因性を持つかどうか(病的バリアントであるかどうか)についての解釈を行うこと。2015年にアメリカ臨床遺伝・ゲノム学会(ACMG)とAssociation for Molecular Pathology (AMP)は、ゲノムのバリアント解釈のガイドラインを共同で発表(Richards et al. Genet Med 17: 405-24, 2015)しており、このガイドラインは、現在多くの専門家と研究者に使用されている。
*9 アノテーション: ここでは、ゲノムの塩基配列やバリアントについて、生物・医学的な注釈付けをすること。
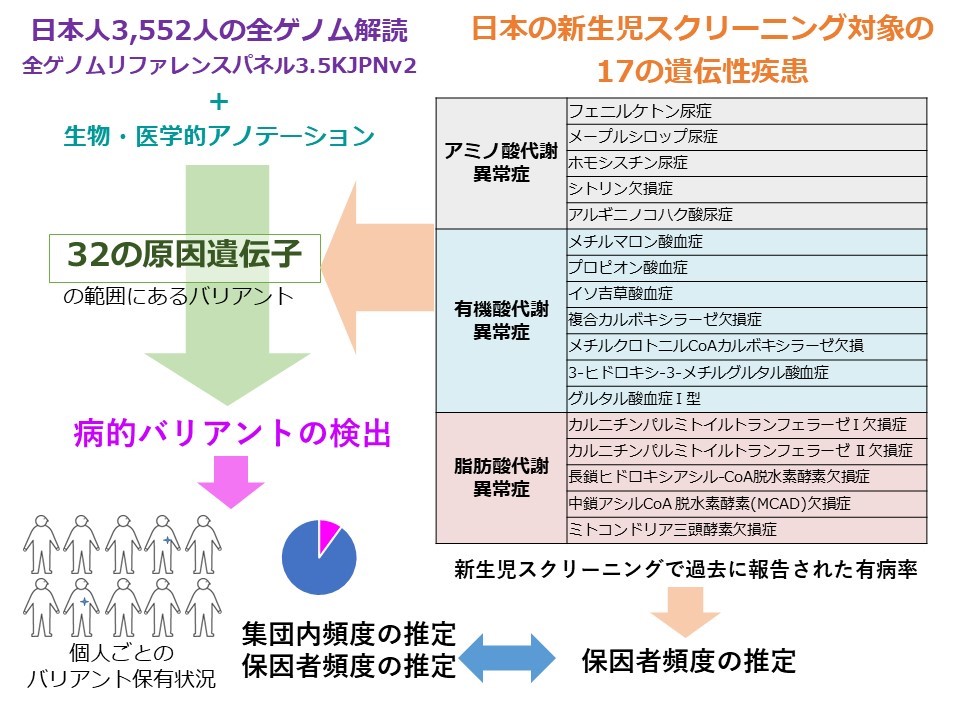
全ゲノムリファレンスパネル3.5KJPNv2のバリアント全体について、医学・生物学的アノテーションを行い、日本の新生児スクリーニング対象疾患の原因となる32の遺伝子を対象に解析を行った。アノテーション情報を活用したバリアント解釈により、病的バリアントの抽出を4種類の方法(病的意義が確からしいバリアントのセットから、病的意義の可能性の候補を含むセット)で行った。検出された病的バリアントから、集団内の頻度、および保因者頻度の推定を行った。
問い合わせ先
(研究に関すること)
東北大学東北メディカル・メガバンク機構
ゲノム解析部門 助教
山口 由美(やまぐち ゆみ)
電話番号:022-274-5952
(報道担当)
東北大学東北メディカル・メガバンク機構
長神 風二(ながみ ふうじ)
電話番号:022-717-7908
ファクス:022-717-7923
Eメール:f-nagami*med.tohoku.ac.jp (*を@に置き換えてください)
