2020年 | プレスリリース・研究成果
難治性耳管開放症患者に対する世界初の治療機器 「耳管ピン」の承認取得 -医師発の治療機器、富士システムズ株式会社との産学連携で製品化へ-
【発表のポイント】
- 産学連携により難治性耳管開放症※1患者に対する治療機器「耳管ピン」を開発し、2017年より多施設共同での医師主導治験※2を実施した。
- 治験の結果、高い有効性と安全性が確認され、2020年5月29日に製造販売承認を取得した※3。
- 難治性耳管開放症患者に対する治療機器としては世界で初めての製品あり、患者さんの苦痛を軽減することが期待される。
【概要】
これまで効果の継続する治療法のなかった難治性耳管開放症に対する治療機器を産学連携により世界で初めて開発しました。
仙塩利府病院の小林俊光医師(東北大学名誉教授)及び 東北大学病院 耳鼻咽喉・頭頸部外科の池田怜吉医師らのグループは、富士システムズ株式会社と難治性耳管開放症患者に対する治療機器「耳管ピン」を開発し、医師主導治験により有効性・安全性が認められ、2020年5月29日に製造販売承認を取得しました。
耳管ピンは、難治性耳管開放症の耳管を閉塞させる機器であり、難治性耳管開放症に対する製造販売承認を取得した治療機器としては、世界で初めての製品です。医師主導治験の結果では、80%以上の患者で改善が認められ、高い有効性・安全性を示しました。
本研究開発は、日本医療研究開発機構(AMED)の臨床研究・治験推進研究事業の日本医師会による研究「医師主導治験の実施支援及び推進に関する研究(2017年~2019年)」の支援を受けて実施されました。また、製品化までの工程では橋渡し研究加速ネットワークプログラムとして東北大学病院臨床研究推進センター(CRIETO)のサポートを受けました。
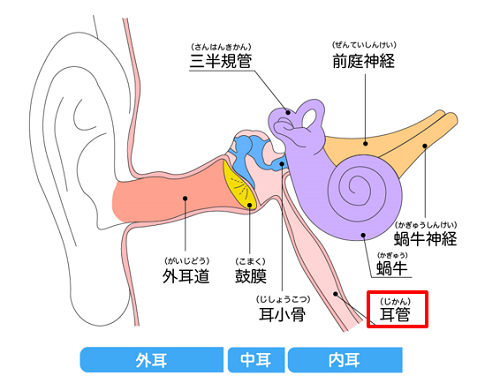
図1.鼓膜の内側にある中耳と鼻の奥を結ぶ耳管(赤枠)
【用語解説】
※1 難治性耳管開放症:強い症状があり、6ヵ月以上の保存的治療(生活指導、生理食塩水を鼻に入れる、漢方薬など)を実施しても改善しない耳管開放症。
※2 多施設共同での医師主導治験:他の医療機関と共同で治験を進める。医師主導治験では、医師自らが治験を企画・立案し、治験計画届けを提出して治験を実施する。
本治験における協力施設は以下の通り。
研究代表:仙塩利府病院 耳科手術センター(センター長 小林俊光)
東北大学病院 耳鼻咽喉・頭頸部外科 (医工学研究科教授 川瀬哲明)
日本大学医学部附属板橋病院 耳鼻咽喉科(教授 大島猛史)
浜松医療センター中耳手術センター(センター長 水田邦博)
※3 製造販売承認:医薬品医療機器等法に基づき、高度管理医療機器を一般流通するにあたって厚生労働大臣から受けなければならない。耳管ピンの承認条件は次の通り。
『耳管開放症の診断及び治療に関連する十分な知識・経験を有する医師が、本品の使用方法に関する技能や手技に伴う合併症等の知識を十分に習得した上で、治療に係る体制が整った医療機関において使用目的及び使用方法を遵守して本品を用いるよう、関連学会と連携の上で必要な措置を講ずること。』
問い合わせ先
東北大学病院広報室
電話番号:022-717-7149
FAX番号:022-717-8931
Eメール:pr*hosp.tohoku.ac.jp(*を@に置き換えてください)
