2019年 | プレスリリース・研究成果
iPS細胞を用いて筋萎縮性側索硬化症の新規病態を発見 - 早期治療標的への応用に期待 -
【発表のポイント】
- 筋萎縮性側索硬化症(ALS)患者より樹立したiPS細胞注1から運動ニューロンを作製し、その運動ニューロンの軸索の形態が異常となることを発見した。
- マイクロ流体デバイス注2とRNAシーケンス注3を組み合わせ、軸索形態異常の原因としてFos-B注4遺伝子を同定した。
- 本研究によりALSの早期治療標的となり得る新たな病態が見出された。
【研究概要】
東北大学東北メディカル・メガバンク機構の秋山 徹也(あきやま てつや)助教、東北大学大学院医学系研究科神経内科学分野の鈴木 直輝(すずき なおき)助教、割田 仁(わりた ひとし)院内講師、青木 正志(あおき まさし)教授、慶應義塾大学医学部生理学教室の岡野 栄之(おかの ひでゆき)教授らの研究グループは、ALS患者由来のiPS細胞を用いてALS運動ニューロンの新たな病態を発見しました。
国の指定難病となっているALSは、全身の運動ニューロンが変性する疾患で、手足の筋肉や呼吸に必要な筋肉がだんだん衰えていく病気です。重篤になると車椅子や人工呼吸器が必要となる場合があります。ALS患者の運動ニューロンでは、ニューロンの細胞体から筋肉へ伸びる「軸索」と呼ばれる突起構造が早期に障害されることが知られています。今回、研究グループは、ALS の原因の一つであるFUS遺伝子に変異を持つiPS細胞から運動ニューロンを作製し、その運動ニューロンの軸索が異常な形態を示すことを発見しました。さらに、新規マイクロ流体デバイスとRNAシーケンスを組み合わせ、運動ニューロンの軸索形態異常にFos-B遺伝子が中心的な役割を担っていることを見出しました。軸索形態異常はALSの神経変性より先に生じていることから、Fos-Bが早期治療標的となることが期待されます。
本研究成果は日本時間2019年6月29日付け(日本時間)で、オープンアクセス学術誌「EBioMedicine」に掲載されました。本研究は国立研究開発法人日本医療研究開発機構(AMED)などの支援を受けて行われました。
【用語説明】
注1. iPS細胞(induced pluripotent stem cell): 人工多能性幹細胞とも言われ、目的細胞へ分化誘導可能な多能性を獲得した細胞。
注2. マイクロ流体デバイス: ここでは、軸索のみが通過可能なマイクロ流路を有する特殊な培養デバイスを指す。ニューロンの細胞体と軸索を分離して培養できるデバイスで、軸索のみの解析が可能。
注3. RNAシーケンス: RNAを網羅的に解析する手法の一つ。
注4. Fos-B:遺伝子発現を調節する転写因子タンパク質の遺伝子。最初期遺伝子と呼ばれる遺伝子群の一つで、神経細胞では神経活動に伴い発現が増えることが知られるが、運動ニューロンでの役割はわかっていない。
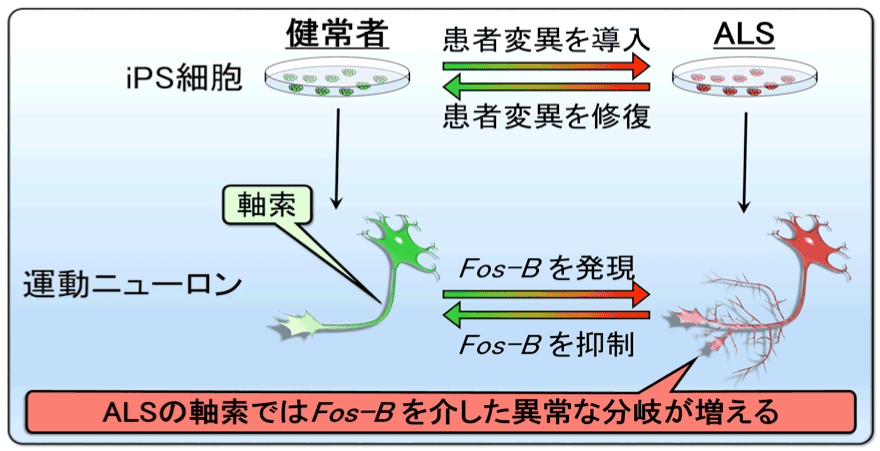
図1. Fos-Bが関与するALS患者運動ニューロンの軸索形態異常
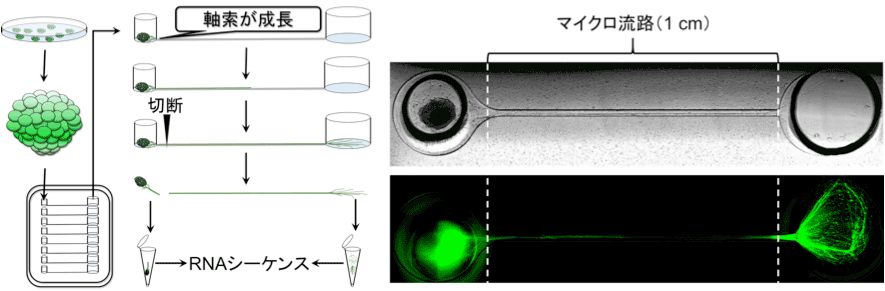
図2. マイクロ流体デバイスを用いた軸索を解析する方法の概要
iPS細胞(左上)から運動ニューロンを作成し、デバイスで培養を行うとマイクロ流路の中を軸索だけが伸びるため、軸索だけを回収して解析できる。右図は、実際に培養した運動ニューロンを示す(上段は位相差画像。下段は運動ニューロンを緑色で標識した画像)。
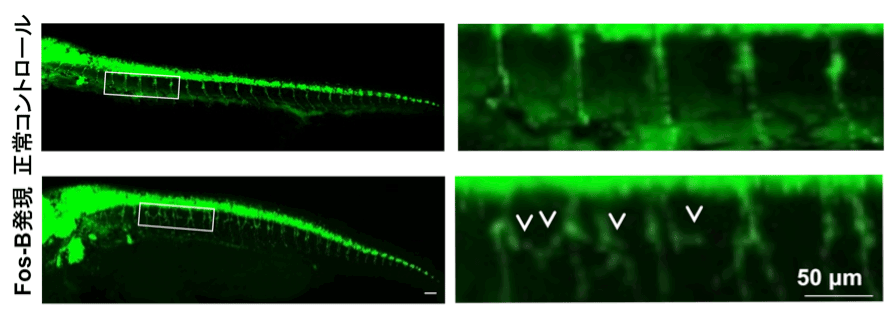
図3. ゼブラフィッシュの運動ニューロン軸索の形態異常 運動ニューロンが緑色に光るゼブラフィッシュ(左列は全体像を示し、白い枠組み部分を右列に拡大して示している)に、Fos-Bを人工的に発現させる(下段)と、軸索の分岐が増える(白矢頭)
問い合わせ先
東北大学大学院医学系研究科神経内科
教授 青木正志(あおきまさし)
助教 鈴木直輝(すずきなおき)
TEL: 022-717-7189
FAX: 022-717-7192
E-mail: aokim*med.tohoku.ac.jp (*を@に置き換えてください)
E-mail: naoki*med.tohoku.ac.jp (*を@に置き換えてください)
(取材に関すること)
東北大学大学院医学系研究科・医学部広報室
TEL: 022-717-7891
FAX: 022-717-8187
E-mail: pr-office@med.tohoku.ac.jp (*を@に置き換えてください)
