2025年 | プレスリリース・研究成果
選択的な糖修飾法を用いて肺非結核性抗酸菌症の治療薬候補を開発 -薬剤耐性菌に有効となる新規抗菌薬開発に期待-
【本学研究者情報】
〇生命科学研究科 助教 横山武司
研究室ウェブサイト
【概要】
慶應義塾大学理工学部応用化学科の高橋大介准教授、戸嶋一敦教授、東北大学大学院生命科学研究科の横山武司助教、微生物化学研究所の五十嵐雅之博士らの研究グループは、マクロライド系抗生物質(※1)アジスロマイシン(AZM)に対する新規化学修飾法の開発を行い、本手法を駆使することで肺非結核性抗酸菌(NTM)症に対する新規リード化合物の創出に成功しました。
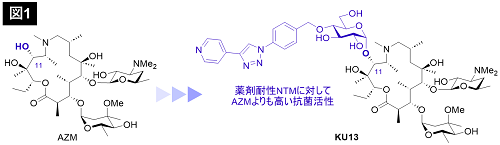
NTMの肺への感染により引き起こされる肺NTM症に対する治療には、AZMが広く利用されていますが、薬剤耐性菌の出現により、新規治療薬の開発が強く求められていました。そこで本研究では、独自に開発してきた位置及び立体選択的グリコシル化反応(※2)を用いて、新規AZM誘導体を迅速に合成する合成法の確立とライブラリーの合成を達成しました。さらに、合成したライブラリーのNTMに対する抗菌活性を評価した結果、誘導体KU13が、薬剤感受性及び薬剤耐性NTMに対してAZMよりも高い抗菌活性を発現することを見出し、本誘導体が新規肺NTM症治療薬候補であることを明らかにしました。また、本誘導体の作用機序解析を行った結果、本誘導体が標的分子であるリボソーム(※3)の構造変化を誘導しながら新しい相互作用を形成する、ユニークな作用機序を明らかにしました。この発見は、薬剤耐性NTMに有効な新たな肺NTM症治療薬の開発への寄与が期待されます。
本研究の成果は、2025年3月5日に、アメリカの総合科学雑誌「Science Advances(サイエンス アドバンシス)」で公開されました。
【用語解説】
※1 マクロライド系抗生物質
多員環ラクトンに糖が結合した抗生物質の総称。細菌のタンパク質合成を阻害することで抗菌作用を発現する。
※2 グリコシル化反応
ある化合物に対して糖を付加する重要な素反応。
※3 リボソーム
遺伝子にコードされた遺伝情報を読み取り、アミノ酸で構成されたタンパク質を合成する、細胞内のタンパク質合成工場。生命の根幹である、セントラルドグマを担うことから生命維持において必須の複合体である。タンパク質合成のプラットフォームの役割を担うのが、RNAとタンパク質で構成される巨大な超分子複合体リボソームである。2000年代初頭にX線結晶構造解析によりその構造の全貌が明らかにされ、結晶化により高分解能構造解析に成功した3名の研究者に2009年にノーベル化学賞が与えられた。抗菌薬の主な標的として知られる。
【論文情報】
タイトル:Creation of a Macrolide Antibiotic against Non-tuberculous Mycobacterium Using Late-stage Boron-mediated Aglycon Delivery,
著者: Yuka Isozaki, Takumi Makikawa, Kosuke Kimura, Daiki Nishihara, Maho Fujino, Yoshikazu Tanaka, Chigusa Hayashi, Yoshimasa Ishizaki, Masayuki Igarashi, Takeshi Yokoyama, Kazunobu Toshima and Daisuke Takahashi,
掲載誌:Science Advances
DOI:doi: 10.1126/sciadv.adt2352
問い合わせ先
(研究に関すること)
東北大学大学院生命科学研究科
助教 横山武司
TEL: 022-217-6206
Email: takeshi.yokoyama.d1*tohoku.ac.jp(*を@に置き換えてください)
(報道に関すること)
東北大学大学院生命科学研究科広報室
高橋さやか
TEL: 022-217-6193
Email: lifsci-pr*grp.tohoku.ac.jp(*を@に置き換えてください)

![]()
東北大学は持続可能な開発目標(SDGs)を支援しています
