2025年 | プレスリリース・研究成果
抗がん抗体活性を100倍向上させるメカニズムを解明 〜構造から読み解く「つなぎ方」の最適設計〜
【本学研究者情報】
〇生命科学研究科 教授 田中良和
研究室ウェブサイト
【発表のポイント】
- がん細胞と免疫細胞を架橋することで免疫応答を誘導する「二重特異性抗体」は次世代の有望ながん治療薬ですが、その設計の際には試行錯誤が避けられません。
- クライオ電子顕微鏡(注1)を用いて、二重特異性抗体を構成する各ドメインの配列順序の変更がもたらす構造変化を明らかにしました。
- 適切なドメイン配列による抗原間、更には細胞間の有利な架橋角度は免疫細胞の誘導効率を高め、抗がん活性を劇的に上昇させます。
【概要】
免疫細胞を利用してがん細胞を攻撃するがん治療抗体の中でも、がん細胞と免疫細胞の抗原を同時に認識し、両細胞を架橋することで強力な免疫応答を誘導する「二重特異性抗体」は、次世代のがん治療法として注目されています。同じ抗体でも設計の違いによって活性が大きく異なることがこれまで、しばしば報告されてきましたが、その理由は分かっていませんでした。
今回、東北大学の田中良和教授、東京農工大学の浅野竜太郎教授、山形大学の真壁幸樹教授らの研究グループは、クライオ電子顕微鏡を使って二重特異性抗体が細胞同士をどのように架橋するかを立体的に捉え、設計の違いによって抗がん活性が100倍以上上昇するメカニズムを解明しました。
本成果は、より効果的ながん治療抗体を合理的に設計するための新たな指針となるものであり、2025年7月14日付で科学誌Cell Reportsに掲載されました。
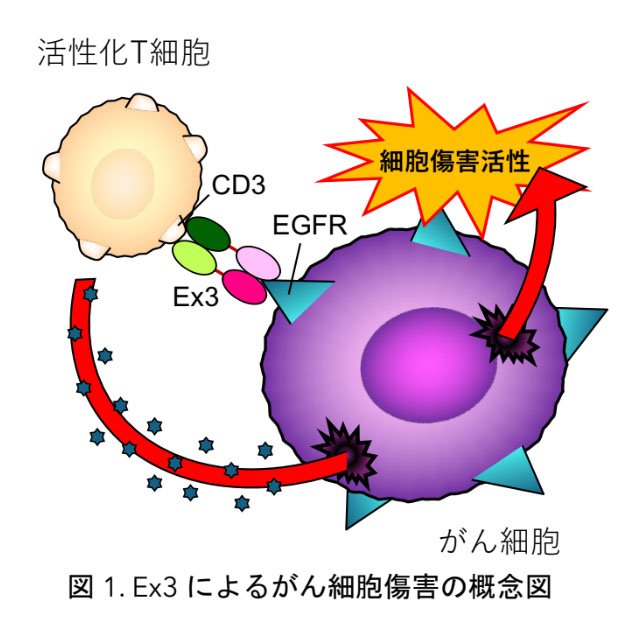
図1. Ex3によるがん細胞傷害の概念図
【用語解説】
注1. クライオ電子顕微鏡
クライオ電子顕微鏡は、ウイルスやタンパク質などの非常に小さな分子を凍らせた状態で観察できる最先端の電子顕微鏡です。試料をグリッドと呼ばれる格子状の金属板の上で急速凍結することで、これらの分子を自然な状態(=生きたままに近い状態)で固定し、観察することができます。
【論文情報】
タイトル:Bispecific antibody-antigen complex structures reveal activity enhancement by domain rearrangement
著者: Kyohei Sato, Shiro Uehara, Atsushi Tsugita, Mayuka Ishii, Shieru Ishiyama, Atsushi Maejima, Ishin Nakahara, Misae Nazuka, Takashi Matsui, Gatsogiannis Christos, Takeshi Yokoyama, Izumi Kumagai, Koki Makabe*, Ryutaro Asano*, and Yoshikazu Tanaka*
*共同責任著者:
東京農工大学 大学院工学研究院生命機能科学部門 教授 浅野竜太郎
山形大学 大学院理工学研究科 教授 真壁幸樹
東北大学 大学院生命科学研究科 応用生命分子解析分野 教授 田中良和
掲載誌:Cell Reports
DOI:10.1016/j.celrep.2025.115965
問い合わせ先
(研究に関すること)
東北大学大学院生命科学研究科
応用生命分子解析分野
教授 田中良和
TEL: 022-217-6205
Email: yoshikazu.tanaka*tohoku.ac.jp(*を@に置き換えてください)
(報道に関すること)
東北大学大学院生命科学研究科広報室
高橋さやか
TEL: 022-217-6193
Email: lifsci-pr*grp.tohoku.ac.jp(*を@に置き換えてください)

![]()
東北大学は持続可能な開発目標(SDGs)を支援しています
