2025年 | プレスリリース・研究成果
肝がん細胞が「セレン代謝」を組み替えて細胞死を回避する仕組みを解明 フェロトーシス誘導治療への抵抗性獲得メカニズムに迫る
【本学研究者情報】
〇大学院薬学研究科 代謝制御薬学分野
教授 斎藤芳郎
研究室ウェブサイト
【発表のポイント】
- セレンは必須微量元素で、抗酸化作用のあるタンパク質を構成しますが、がん細胞では、この抗酸化作用が逆に生存や増殖を助けることがあります。
- 肝細胞がんでは、酸化ストレスに応答する転写因子NRF2により、セレンを細胞外に運ぶタンパク質セレノプロテインP(SeP)が減少することがわかりました。
- SePの減少により、細胞内のセレンが増え、抗酸化作用を持つタンパク質が増加し、その結果、がん細胞は酸化ストレスによる細胞死(フェロトーシス)に強くなり、治療への抵抗性を高める可能性が示されました。
【概要】
セレンは体内で活性酸素を除去する抗酸化酵素などの構成成分として重要な役割を果たす必須微量元素であり、健康維持に欠かせません。その中でも「セレノプロテインP(SeP)」は肝臓で合成され、全身にセレンを輸送する特殊なタンパク質です。近年、肝細胞がんでSeP発現が低下していることが報告されていますが、その減少の理由やがん細胞の生存戦略との関連は不明でした。
東北大学大学院薬学研究科の有澤琴子助教、平沼哲太(当時学部学生)、名取萌花(当時学部学生)、斎藤芳郎教授らの研究グループは、single-cell RNAシーケンス解析と培養細胞実験により、酸化ストレス応答転写因子NRF2が肝がん細胞でSeP発現を抑制することを発見しました。さらに、このSeP減少は細胞外へのセレン分泌を抑える一方で細胞内セレン量を増加させることで、抗酸化セレンタンパク質(GPx1やGPx4)の発現を促進してフェロトーシス(鉄依存的な細胞死)を抑制することを明らかにしました。
この成果は、がん細胞が細胞内のセレンの量を増やすことで、酸化ストレスによる細胞死を巧みに回避している仕組みを示すものです。また、がん細胞がフェロトーシス誘導治療に抵抗する新たなメカニズムを提示するとともに、SePを介したセレン利用の制御が治療戦略の開発において重要な手がかりとなることを示しています。
本成果は、2025年8月13日、学術誌 Redox Biology に掲載されました。
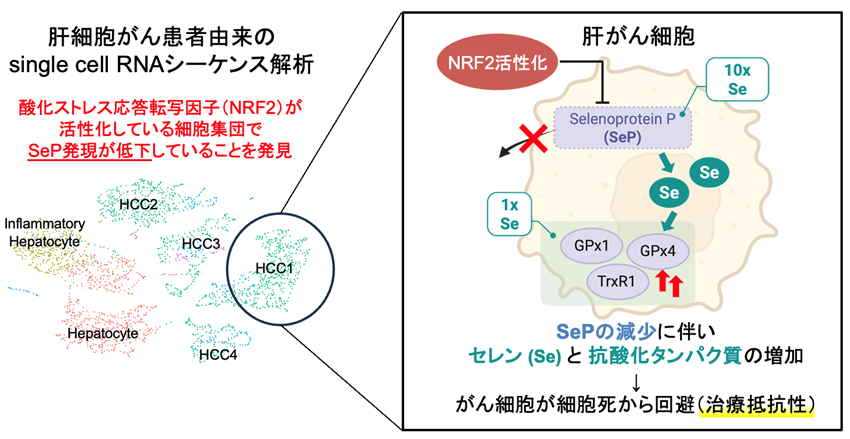
図1. 本研究の概要
【論文情報】
タイトル:NRF2-dependent suppression of selenoprotein P expression promotes intracellular selenium metabolic remodeling and upregulation of antioxidant selenoproteins in hepatocellular carcinoma
*責任著者:東北大学大学院薬学研究科 教授 斎藤芳郎
掲載誌:Redox Biology
DOI:10.1016/j.redox.2025.103821
問い合わせ先
(研究に関すること)
東北大学大学院薬学研究科
代謝制御薬学分野
教授 斎藤芳郎
TEL:022-795-6870
Email: Yoshiro.saito.a8*tohoku.ac.jp
(*を@に置き換えてください)
(報道に関すること)
東北大学大学院薬学研究科
総務係
TEL: 022-795-6801
Email: ph-som*grp.tohoku.ac.jp
(*を@に置き換えてください)

![]()
東北大学は持続可能な開発目標(SDGs)を支援しています
