2023年 | プレスリリース・研究成果
鉄触媒と酸素でペプチドを自在につなぐ反応の開発 ペプチドの二量化を基盤とした創薬開発への貢献に期待
【本学研究者情報】
〇薬学研究科 医薬製造化学分野
教授 徳山英利
研究室ウェブサイト
【発表のポイント】
- アミノ酸の一つであるトリプトファン同士を結合させる注1の開発に成功しました。
- 酸素の中で、低毒性で天然に豊富に存在する鉄を中心に有する触媒を用いた環境にやさしい反応です。
- アミノ酸側鎖を保護注2することなく、ペプチドを直接利用可能な常識を破る反応です。
- 様々なトリプトファン含有ペプチド二量体の合成により医薬品の創出に期待されます。
【概要】
アミノ酸の一種であるトリプトファンは、自然界で二量化という化学反応を起こすことが知られています。カビなどの微生物は、医薬品として有用な活性を示す化合物をこの反応を利用して産出しています。ヒトの体内においても、この化学反応を契機としてタンパク質凝集体が形成され、様々な疾病の発現に関与していると考えられています。これまで多くの有機化学者がトリプトファンやトリプトファンを含有するペプチドの二量化のフラスコ内での再現を目指す研究を行ってきました。しかしトリペプチド以上の複雑なペプチドのトリプトファン部位で結合する二量化反応は、未開発でした。
東北大学大学院薬学研究科 徳山英利教授と植田浩史講師らの研究グループは、トリプトファン部位で結合するペプチドの画期的な二量化法の開発に成功しました。研究グループは生体酵素をヒントにした鉄触媒を用いることで、単純なトリプトファンから生理活性オリゴペプチドまで、幅広い化合物を無保護のまま用いて二量化できる、従来にはない画期的反応を実現しました。本手法は酸素を酸化剤とし、低毒性かつ天然に豊富な鉄を有する触媒を用いた環境調和性に優れた手法です。従来の常識では考えられなかった無保護のペプチドの二量化の実現は、今後の創薬研究の発展や病理学的メカニズムの解明に繋がることが期待されます。
本研究の成果は、2023年3月24日付でドイツ化学会誌Angewandte Chemie International Editionにオンライン掲載されました。
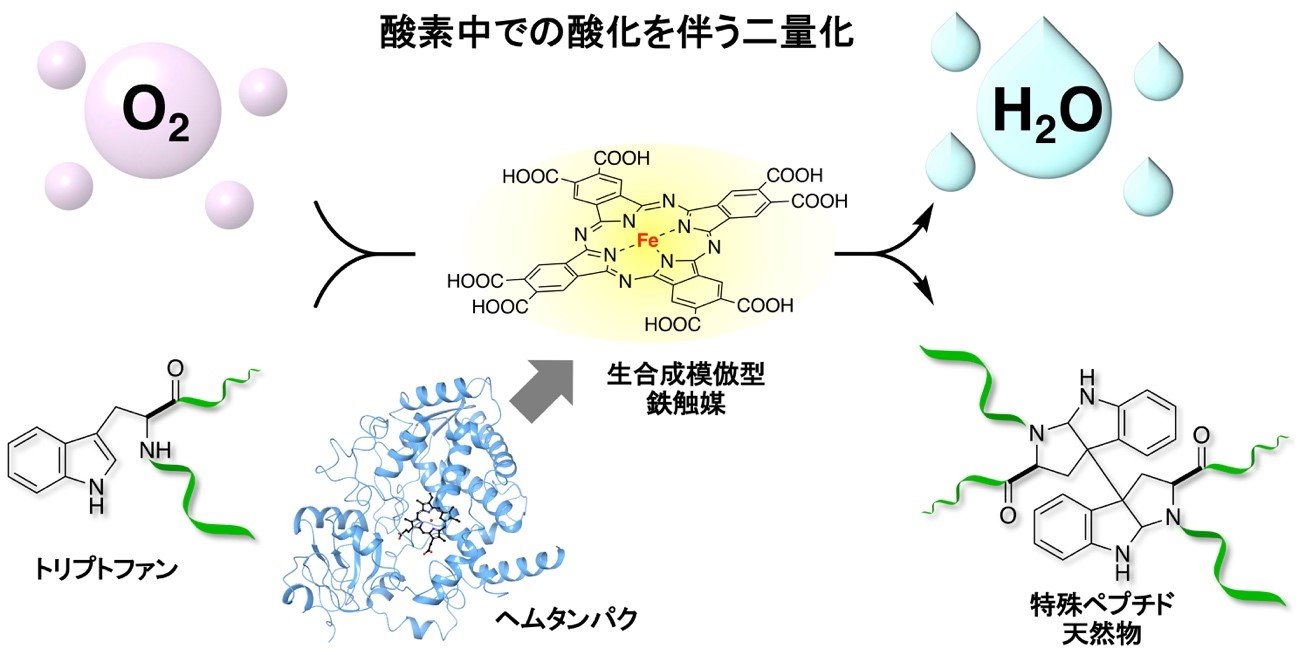
図1. 本研究の概要:ヘムタンパクを模倣した鉄触媒によって酸素中でペプチドのトリプトファン同士が結合する画期的な二量化反応
【用語解説】
(注 1)二量化反応:
2つの同一または類似の分子が新たな結合を形成して連結する反応。
(注 2)保護:
反応性の高い部位を他の構造に変換することで、試薬に対して反応しなくすること。通常、その後の脱保護操作によって元の形に戻す。保護、脱保護の2段階を行うと、合成の段階数が増えて効率性が低下する。
問い合わせ先
(研究に関すること)
東北大学大学院薬学研究科
教授 徳山英利
電話: 022-795-6887
E-mail: hidetoshi.tokuyama.d4*tohoku.ac.jp(*を@に置き換えてください)
講師 植田浩史
電話: 022-795-6878
E-mail: hirofumi.ueda.d8*tohoku.ac.jp(*を@に置き換えてください)
(報道に関すること)
東北大学大学院薬学研究科・薬学部 総務係
電話: 022-795-6801
E-mail: ph-som*grp.tohoku.ac.jp(*を@に置き換えてください)

![]()
![]()
![]()
東北大学は持続可能な開発目標(SDGs)を支援しています
