2025年 | プレスリリース・研究成果
アミノ酸/ペプチドへのジスルフィド連結法を開発 創薬や薬物送達への利用につながる成果
【本学研究者情報】
〇大学院薬学研究科 分子設計化学分野
教授 吉戒直彦
助教 金本和也
研究室ウェブサイト
【発表のポイント】
- 2つの硫黄原子がつながるジスルフィド構造(注1)は、創薬研究や生体内の薬物送達などにおいて重要です。しかし、アミノ酸やペプチド(注2)のα位にジスルフィド結合を導入する手法は未開拓でした。
- アミノ酸等価体のアズラクトン(注3)に対して、穏和にジスルフィド構造を導入できる反応の開発に成功しました。アミノ酸部位は更なる変換が可能であり、機能性分子の連結やペプチド鎖の伸長に利用できます。
- 本手法により、アミノ酸誘導体やペプチドのα位にジスルフィドを介して医薬品分子や蛍光分子などの有用な化合物を連結できるため、生命科学研究への貢献が期待されます。
【概要】
ジスルフィド構造は、創薬研究に加えて、生体内で切断可能な連結部(リンカー)として薬物送達などにも利用されています。そのため、ジスルフィド構造に、多彩な生体分子を構成するアミノ酸やペプチドを導入する手法の開発が求められています。しかし、ジスルフィド試薬が未発展であることもあり、アミノ酸やペプチドのα位にジスルフィド結合を連結することは困難でした。
東北大学大学院薬学研究科の金本和也 助教、吉戒直彦 教授、岩田真輝 大学院生、鷹見優月 大学院生、浅沼隼人 大学院生、大野響己 学部生と、中央大学大学院 理工学研究科の細野兼矢 大学院生らの研究グループは、アミノ酸等価体のアズラクトンに対してジスルフィド構造を導入する反応の開発に成功しました。本手法は幅広いジスルフィドの合成に利用できるのみならず、開環を伴う更なる変換によってペプチド鎖や医薬品分子など多彩な有用化合物に連結できるため、創薬研究や薬物送達などへの利用を通じて、さまざまな生命科学研究に寄与するものと期待されます。
本研究成果は2025年1月7日付で科学誌 Chemical Science にオンライン掲載されました。
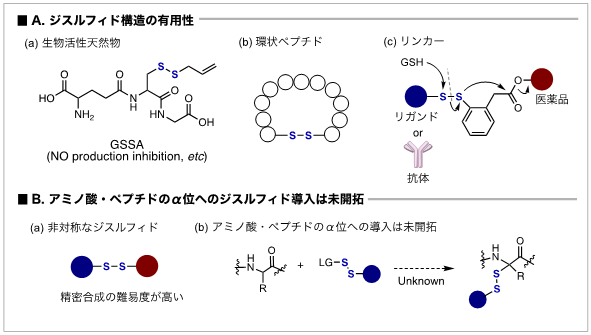
図1. アミノ酸やペプチドのα位へのジスルフィド導入の背景
【用語解説】
注1. ジスルフィド構造は、2つの硫黄原子が連続した構造をあらわす。多彩な生物活性天然物にみられるほか、ペプチドの三次元構造の制限を目的とした環状ペプチド形成や、生体内で切断可能なリンカーとしての利用など、多彩な応用が期待されている。
注2. ペプチド構造は、複数のアミノ酸がペプチド結合(-CONH-)を介して連結された分子のことで、多彩な生命現象に関与する。タンパク質も連続する多数のペプチド結合によって構成される。α位とは、アミノ酸の中心炭素(α炭素)の位置を指し、この炭素はアミノ基とカルボキシル基、および側鎖(R基)が結合している。ペプチド結合を形成する際、α炭素はアミド結合に隣接している。
注3. アズラクトンは環状のアミノ酸等価体であり、α位のプロトンの酸性度の高さから穏和な条件で利用できるため非天然アミノ酸の合成に用いられる。開環反応によって更なる連結を行える点も利点として挙げられる。
【論文情報】
タイトル:A versatile entry to unnatural, disulfide-linked amino acids and peptides through the disulfuration of azlactones
著者: Masaki Iwata, Yuzuki Takami, Hayato Asanuma, Kenya Hosono, Hibiki Ohno, Naohiko Yoshikai, Kazuya Kanemoto*
*責任著者:東北大学大学院薬学研究科 助教 金本和也
掲載誌:Chemical Science
DOI:10.1039/D4SC07187E
問い合わせ先
(研究に関すること)
東北大学大学院薬学研究科
助教 金本和也
TEL: 022-795-6815
Email: kazuya.kanemoto.a1*tohoku.ac.jp
(*を@に置き換えてください)
(報道に関すること)
東北大学大学院薬学研究科 総務係
TEL: 022-795-6801
Email: ph-som*grp.tohoku.ac.jp
(*を@に置き換えてください)

![]()
東北大学は持続可能な開発目標(SDGs)を支援しています
