2026年 | プレスリリース・研究成果
がん抑制遺伝子p53を強く活性化する新たな抗がん治療の鍵分子MKRN1の発見 ―抗がん剤耐性がんに対する新規治療戦略に期待―
【本学研究者情報】
〇薬学研究科衛生化学分野 教授 松沢厚
研究室ウェブサイト
【発表のポイント】
- 細胞のがん化を防ぐために最も重要なDNA損傷応答(注1)を制御する新規因子としてMKRN1 (Makorin Ring Finger Protein 1)を発見しました。
- MKRN1は、DNA損傷応答を担うp53の働きをコントロールすることで、適切なDNA損傷応答を誘導していることを明らかにしました。
- MKRN1によるDNA損傷応答に異常があると、シスプラチン(注2)などの抗がん剤の効果が著しく低下することから、MKRN1はがん治療効果を左右する重要な因子であることが示されました。
- 本研究成果は、抗がん剤への治療抵抗性を示すがんに対する新たな治療法の確立に繋がると考えられます。
【概要】
DNA損傷応答は、細胞ががん化を防ぐために備える最も重要なシステムの一つです。その中心的役割を担うp53は、定常時にはMDM2により速やかに分解されており、必要な時にだけ活性化される精密なフィードバック制御機構によって守られています。
東北大学大学院薬学研究科の島田竜耶博士、小松龍斗大学院生、大谷航平大学院生、松沢厚教授および岩手医科大学薬学部の野口拓也教授らの研究グループは、これを調節する新たな分子としてE3ユビキチンリガーゼ(注3)MKRN1を同定しました。MKRN1は定常時にp53を分解することでその発現を制御する一方で、DNA損傷が起こるとMDM2を選択的に分解へと導き、p53の活性化を促進するという二面性を持つ分子であることを明らかにしました。
本研究の成果は、2026年1月30日に細胞死に関する専門誌 Cell Death & Differentiationに掲載されました。
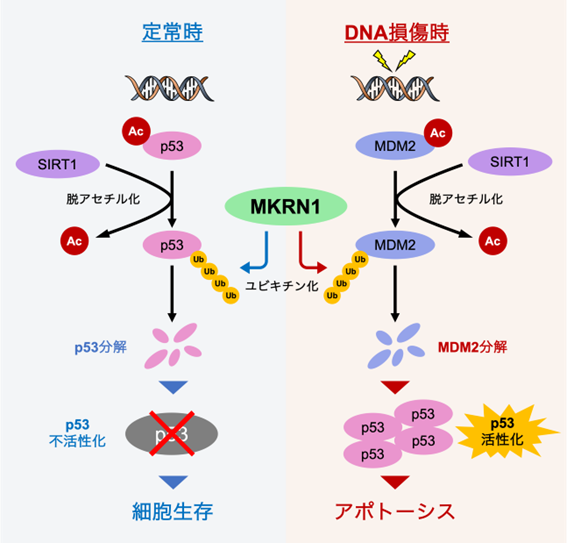
図1. MKRN1によるp53-MDM2制御系の調節機構
定常時、MKRN1はSIRT1によって脱アセチル化されたp53をユビキチン化分解することでその発現量を低く保っている。一方でDNA損傷時には、MKRN1はSIRT1によって脱アセチル化されたMDM2に基質を切り替え、MDM2をユビキチン化分解することで、p53の活性化を起こしアポトーシスを誘導する。
【用語解説】
注1. DNA損傷応答
DNAが損傷を受けた際に細胞が働かせる防御システム。損傷の修復や細胞周期の停止、p53依存的なアポトーシスの誘導などを行うことで、細胞のがん化を防いでいる。
注2. シスプラチン
代表的なDNA損傷型の抗がん剤。DNAに結合して構造異常を引き起こし、細胞死を誘導する。
注3. E3ユビキチンリガーゼ
ユビキチンという小さなタンパク質を特定の標的タンパク質に付加して「分解の目印」をつける酵素。細胞内タンパク質の寿命や品質管理などにおいて中心的な役割を果たす。
【論文情報】
タイトル:Identification of MKRN1 as a key modulator of the p53-MDM2 feedback loop
著者:†Shimada T, †*Noguchi T, †Komatsu R, †Otani K, Komatsu T, Suzuki S, Mitsuya M, Okubo T, Ito R, Yamada M, Hirata Y, *Matsuzawa A.
†筆頭著者:東北大学大学院薬学研究科 大学院生 (研究当時)島田竜耶
東北大学大学院薬学研究科 大学院生 小松龍斗
東北大学大学院薬学研究科 大学院生 大谷航平
†筆頭著者 *責任著者:岩手医科大学薬学部 教授 野口拓也
*責任著者:東北大学大学院薬学研究科 教授 松沢厚
掲載誌:Cell Death & Differentiation
DOI:10.1038/s41418-026-01662-4
問い合わせ先
(研究に関すること)
東北大学大学院薬学研究科
教授 松沢厚
TEL: 022-795-6827
Email: atsushi.matsuzawa.c6*tohoku.ac.jp(*を@に置き換えてください)
(報道に関すること)
東北大学大学院薬学研究科
総務係
TEL: 022-795-6801
Email: ph-som*grp.tohoku.ac.jp(*を@に置き換えてください)

![]()
東北大学は持続可能な開発目標(SDGs)を支援しています
